Reino Unido: las personas con alergias severas quedan fuera de la vacunación
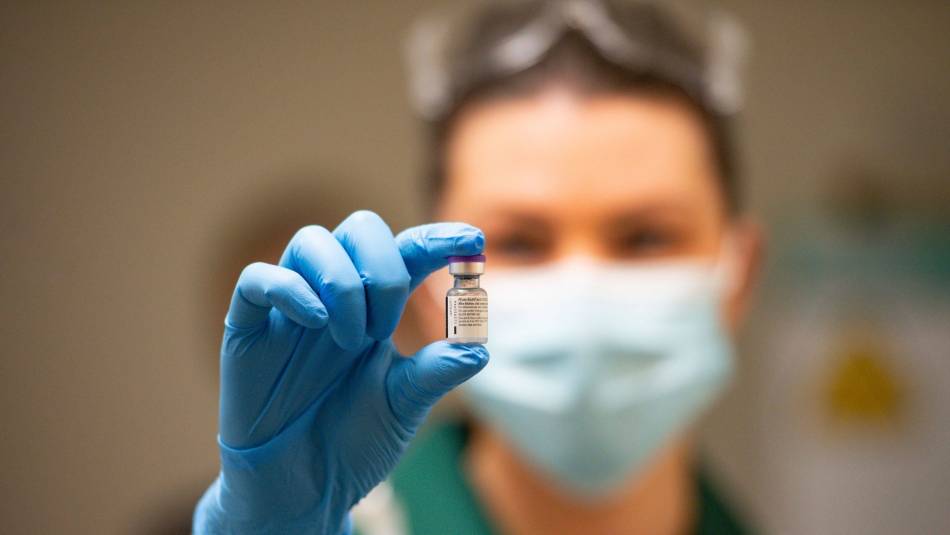
La advertencia se produce luego de que dos personas experimentaran reacciones a la inoculación de Pfizer.
Las personas con importantes antecedentes de alergias no deben vacunarse actualmente con el tratamiento contra el Covid-19 de Pfizer Inc. y BioNTech SE, señaló el Servicio Nacional de Salud (NHS, por sus siglas en inglés) del Reino Unido, después de que dos personas experimentaran reacciones a la vacuna.
La advertencia realizada el miércoles se produjo un día después de que el Reino Unido se convirtiera en la primera nación occidental en comenzar un programa de vacunación contra el Covid, luego de que la semana pasada la Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) del país autorizara la vacuna.
Fauci critica la rápida aprobación de la vacuna en Reino Unido… y los británicos responden
Precaución
“Como es común con las nuevas vacunas, la MHRA aconsejó como precaución que no se administre esta vacuna a las personas con importantes antecedentes de reacciones alérgicas”, dijo Stephen Powis, director médico nacional del NHS en Inglaterra, en un comunicado.
June Raine, directora ejecutiva de la MHRA, dijo que el martes por la noche su equipo analizó dos informes de casos de reacciones alérgicas. Ambas personas, empleados del NHS, se están recuperando satisfactoriamente, indicó el servicio de salud.
“Sabemos por los extensos ensayos clínicos que esto no era una característica, que si necesitamos fortalecer nuestro consejo ahora que ya tenemos esta experiencia en las poblaciones vulnerables, lo llevaremos a la población de inmediato”, dijo Raine a un panel de legisladores.
El paso a paso británico para su vacunación
Pfizer y BioNTech dijeron que están prestando apoyo a la MHRA en su investigación.
La agencia del Reino Unido ya había advertido en su información de prescripción que no debería administrarse esta vacuna a personas que son alérgicas a cualquier ingrediente contenido en ella. Los pacientes con antecedentes de reacciones adversas graves a una vacuna o reacciones alérgicas graves a cualquier componente del tratamiento fueron excluidos de participar en el gran estudio realizado por las empresas antes de su aprobación.
“En el crucial ensayo clínico de fase 3, esta vacuna fue generalmente bien tolerada; el comité independiente de monitoreo de datos no alertó de preocupaciones serias de seguridad”, dijeron las compañías en un comunicado.
{{noticia:94554}

